Comment Calculer La Masse Molaire
- Quantité de matière et concentration molaire Flashcards | Quizlet
- Masse molaire de l'AIR : exercice de sciences physiques de seconde - 229718
- Calculateur de masse molaire, poids moléculaire et composition élementaire
À partir des concentrations atomiques n Ti et n Al, on a * la masse d'aluminium dans une mole de Ti3Al, m Al = n AlMAl; * la masse d'une mole de Ti3Al, m Ti3Al = n AlMAl + n TiMTice qui nous permert de calculer la concentration massique d'aluminium: Par ailleurs, la somme des teneurs donne 100% donc n Ti = 100 - n Al et donc:; Énoncé Le perlite est un alliage de fer et de carbone contenant 0, 77%m de carbone. Quelle est le pourcentage atomique de carbone? ; Données Masses molaires atomiques (ou masses atomiques): * carbone: MC = 12 g/mol (voir Carbone sur Wikipédia); fer: MFe= 56 g/mol (voir Fer sur Wikipédia). Pourcentage atomique de la perlite Le problème est le symétrique du problème précédent. On part de la même équation, qu'il faut inverser: la concentration massique de carbone vaut: Par ailleurs, la somme des teneurs donne 100% donc n Fe = 100 - n C et donc: soit Capacité calorifique [ modifier | modifier le wikicode] La capacité calorifique à pression constante, ou capacité thermique à pression constante, mesure la chaleur (en joules) qu'il faut apporter à une quantité de matière pour élever sa température de 1 °C (ou 1 K, ce qui est la même chose).
Quantité de matière et concentration molaire Flashcards | Quizlet
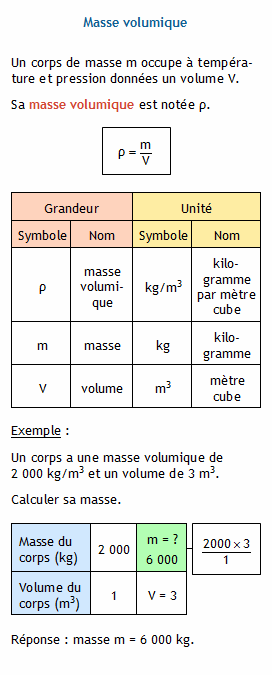


Masse molaire de l'AIR : exercice de sciences physiques de seconde - 229718
L'atome de soufre lui a une masse molaire de 32. 1 g/mol. L'atome de platine, 195. 1 g/mol... 5. Pour calculer la masse molaire d'une molécule, il suffit d'additionner la masse de chaque atome la composant. 6. Par exemple, notre brave glucose C6 H12 O6... Il contient 6 atomes de carbone. Or, d'après le tableau de Mendeleiev, la masse molaire de carbone est de 12 g/mol. Donc, nous multiplions le nombre d'atomes de carbone, par sa masse molaire: 6 * 12 = 72 g/mol. 7. Le glucose contient 12 atomes d'hydrogène. Or, la masse molaire d'un atome d'hydrogène est de 1 g/mol. 12 * 1 = 12 g/mol. 8. Et enfin, le glucose contient 6 atomes d'oxygène, dont la masse molaire est de 16 g/mol. Donc: 6 * 16 = 96 g/mol. 9. Pour connaître la masse molaire de la molécule de glucose, nous ajoutons la masse molaire de l'ensemble des atomes de carbone, d'hydrogène et d'oxygène. 10. La masse molaire du glucose est donc: (6x12) + (12x1) + (6x16) = 180g/mol 72 + 12 + 96 = 180 g/mol. 11. Le fonctionnement est identique pour des molécules plus complexes.
- Ent normandie caen
- Terrain a vendre 06 2
- Bicarbonate de soude : comment l'utiliser ? Quels sont ses bienfaits ?
- Comment calculer la masse molaire d'un ion ? - Quora
Des exemples de calculs de masse moléculaire: C[14]O[16]2, S[34]O[16]2. Définitions de la masse moléculaire, le poids moléculaire, la masse molaire et le poids molaire La masse moléculaire ( poids moléculaire) est la masse d'une molécule d'une substance et est exprimée en unités de masse atomique unifiée (u). (1 u est égal à 1/12 de la masse d'un atome de carbone-12) La masse molaire ( masse molaire) est la masse d'une mole d'une substance et est exprimée en g / mol. Le poids des atomes et isotopes sont de l' article NIST. Laissez-nous vos commentaires de votre expérience avec la Calculatrice Poids Moléculaire. Connexes: les poids moléculaires href=''>
Calculateur de masse molaire, poids moléculaire et composition élementaire
La masse d'une mole d'atomes d'or (ou |6, 023 \times 10^{23} \space \text {atomes}|) est 196, 967 g d'or (Au). Il est possible de calculer le nombre d'atomes pour un élément donné en utilisant la relation mathématique suivante: |\displaystyle n = \frac {m}{M}| où n représente le nombre de mole(s) (d'atomes ou de molécules) en mole (mol) m représente la masse de l'échantillon (ou masse expérimentale) exprimée en grammes (g) M représente la masse molaire (atomique ou moléculaire) telle que calculée à partir du tableau périodique et exprimée en grammes par mole (g/mol) Combien de moles y a-t-il dans 0, 24 g de carbone (C)? Combien d'atomes y a-t-il dans cette même quantité? Pour répondre à la première question, il faut utiliser la formule ci-dessus. |n =? | |m = 0, 24 \space \space \text {g}| |M= 12, 011 \space \text {g/mol}| (selon la valeur indiquée dans le tableau périodique) |\displaystyle n = \frac {m}{M}| |\displaystyle n = \frac {0, 24 \space \text {g}}{12, 011 \space \text {g/mol}}| |\displaystyle n = 0, 02 \space \text {mol}| Pour déterminer le nombre d'atomes, il faut utiliser le nombre d'Avogadro.
Définition d'une mole La mole est la grandeur qui permet de quantifier la matière. Les atomes et les molécules étant très petits et donc très légers, l'idée est d'en faire un "paquet", pour arriver à travailler sur des masses comprises entre 1 et des dizaines de grammes (des ordres de grandeur que nous avons l'habitude de manipuler). La mole a ainsi été définie à partir d'un élément très connu: le carbone 12. Pour constituer un système de 12 grammes de carbone 12, il faut 602 200 000 000 000 000 000 000 atomes de carbone, soit 6, 022 x 10 23. Ce nombre est appelé nombre d'Avogadro. RETENIR: une mole est la quantité de matière d'un système contenant autant d'entités élémentaires qu'il y a d'atomes dans 12 g de carbone 12. NOTER: le nombre d'Avogadro est le nombre d'entités contenues dans une mole d'entités. N A = 6, 022 x 10 23. Exemple pour un atome: une mole d'oxygène est un ensemble de 6, 022 x 10 23 atomes d'oxygène. Exemple pour une molécule: une mole de molécules de dihydrogène est un ensemble de 6, 022 x 10 23 molécules de dihydrogène.